Mieloma multiplo recidivato: isatuximab disponibile anche in Italia come trattamento di seconda linea
- L’associazione, ad oggi l’unica rimborsata in Italia, di isatuximab alla terapia standard con carfilzomib e desametasone ha dimostrato di ridurre significativamente il rischio di progressione o morte rispetto al solo standard di cura
- Questa associazione rappresenta un’ulteriore opportunità per pazienti che hanno ricevuto almeno una terapia precedente
- È un’ulteriore conferma per isatuximab, molecola al centro di un ampio programma di sviluppo clinico di Sanofi nel mieloma multiplo
L’Agenzia Italiana del Farmaco (AIFA) ha pubblicato in Gazzetta Ufficiale la determina di rimborsabilità per l’utilizzo dell’anticorpo monoclonale isatuximab in combinazione allo standard di cura rappresentato da carfilzomib e desametasone (Kd), come trattamento in pazienti adulti con mieloma multiplo che hanno ricevuto almeno una precedente terapia.
Si tratta della seconda indicazione di isatuximab disponibile in Italia in meno di 12 mesi e si basa sui dati dello studio di fase 3 IKEMA, uno studio clinico randomizzato, multicentrico e in aperto che ha arruolato 302 pazienti con mieloma multiplo recidivato in 69 centri e 16 Paesi. Da questo studio emerge che la terapia in combinazione con isatuximab è in grado di ridurre il rischio di progressione di malattia o morte del 47% rispetto alla terapia standard con carfilzomib e desametasone (Kd).
Michele Cavo Direttore dell’Istituto di Ematologia “Seràgnoli” IRCCS Azienda Ospedaliero-Universitaria di Bologna, Principal Investigator dello studio IKEMA in Italia
“Per una patologia complessa e caratterizzata da multiple ricadute come il mieloma multiplo, è fondamentale continuare a ricercare e sperimentare nuove combinazioni e opzioni di trattamento che possano prolungare l’aspettativa di vita con minore rischio di progressione della malattia. Questo nuovo regime va quindi ad arricchire le opzioni terapeutiche a disposizione degli specialisti e dei pazienti italiani con mieloma multiplo recidivato che possono oggi beneficiare di un’efficace arma in più al momento della prima recidiva”.
Il provvedimento dell’AIFA arriva oggi in seguito all’approvazione da parte della European Medicines Agency (EMA) per isatuximab avvenuta nel 2021. Anche la Food and Drug Administration (FDA) statunitense ha approvato questa associazione nel 2021.
Da ottobre 2021, isatuximab è disponibile in Italia come trattamento in terza linea, in combinazione con un altro regime standard di cura, pomalidomide e desametasone (pom-dex), come trattamento in pazienti adulti con mieloma multiplo recidivato e refrattario che hanno ricevuto almeno due terapie precedenti tra cui lenalidomide e un inibitore del proteasoma e hanno registrato una progressione della malattia a seguito dell’ultima terapia.
Mariangela Amoroso Country Medical Lead di Sanofi in Italia
“Come Sanofi siamo impegnati nello sviluppo di molecole antitumorali innovative; tra gli altri, anticorpi di nuova generazione che reclutano il sistema immunitario dell’organismo attivandolo specificatamente contro le cellule tumorali. La nostra ricerca si concentra soprattutto in quattro aree: i tumori cutanei non melanoma, il tumore del polmone, della mammella ed il mieloma multiplo che rappresenta una sfida terapeutica considerevole perché progressivo, complesso e tutt’oggi incurabile. Grazie ad un articolato programma di studi clinici in cui anche il nostro Paese è stato ampiamente coinvolto, è stato possibile mettere a disposizione questa nuova soluzione terapeutica”.
Il mieloma multiplo
Il mieloma multiplo è la seconda neoplasia del sangue per diffusione[i]. Ogni anno si registrano più di 130.000 nuove diagnosi al mondo[ii], circa 39.000 in Europa[iii]. Nonostante i trattamenti disponibili, il mieloma multiplo rimane un tumore maligno incurabile che, si accompagna ad un significativo impatto sulla vita dei pazienti, per lo più anziani. Infatti, la maggior parte dei pazienti con mieloma multiplo va incontro ad una ricaduta. Il mieloma multiplo si definisce recidivato quando si ripresenta dopo un trattamento o un periodo di remissione; è invece refrattario quando non risponde o smette di rispondere alla terapia.
Isatuximab
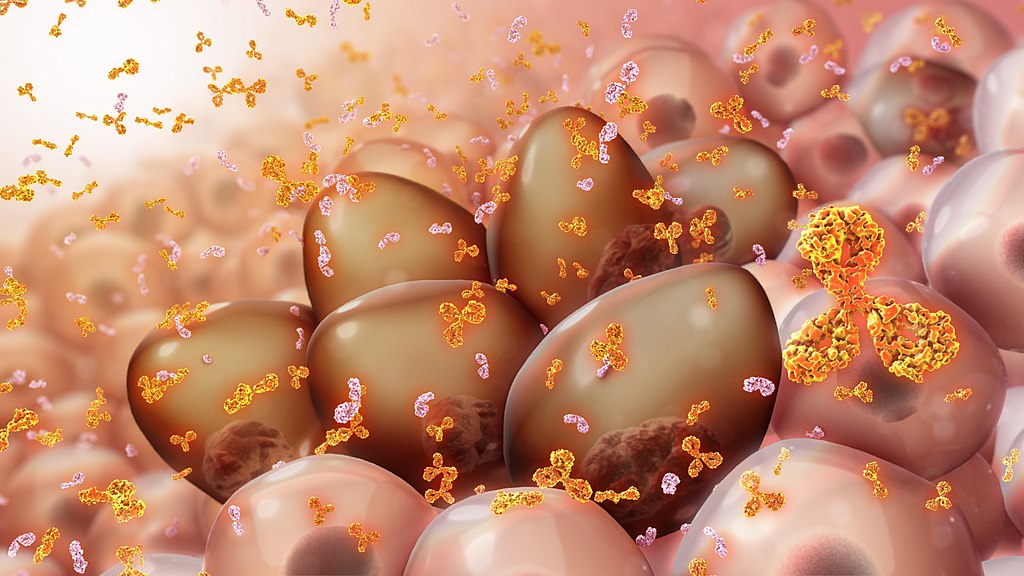
Isatuximab è un anticorpo monoclonale che si lega a un epitopo specifico sul recettore CD-38 delle cellule tumorali. È progettato per funzionare attraverso molteplici meccanismi d’azione, tra cui la morte programmata delle cellule tumorali (apoptosi) e l’attività immunomodulatoria. Il recettore CD-38 è altamente e uniformemente espresso sulla superficie delle cellule affette da mieloma multiplo, tanto da essere un potenziale bersaglio per le terapie a base di anticorpi come isatuximab.
Isatuximab è in sperimentazione anche come trattamento in prima linea, in altri studi clinici di fase 3, in combinazione con i trattamenti standard disponibili per la terapia del mieloma multiplo, oltre a essere in sperimentazione nel trattamento di altre neoplasie ematologiche.
[i] Kazandjian. Multiple myeloma epidemiology and survival: A unique malignancy. Semin Oncol. 2016;43(6):676-681. doi:10.1053/j/seminoncol.2016.11.004
[ii] International Myeloma Foundation. Myeloma Action Month. https://mam.myeloma.org/learn-more-about-multiple-myeloma/. Accessed February 2021. 2/6.
[iii] João C, Costa C, Coelho I, Vergueiro MJ, Ferreira M, Silva MG. Long‐term survival in multiple myeloma. Clinical Case Reports. 2014;2(5):173-179. doi:10.1002/ccr3.76. 3. Schey SA, Morris J, Maguire Á, Dhanasiri
immagine di copertina: By www.scientificanimations.com – http://www.scientificanimations.com/wiki-images/, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=78285125